

POR VIMAN SISTEMAS | Publicado em 20 de junho de 2020
- Responsabilidade Gerencial
- Gerenciamento de Riscos
- Controle de Compras
Os profissionais Responsáveis Técnicos enfrentam diariamente inúmeras preocupações que estão diretamente relacionadas ao cumprimento efetivo da gestão regulatória e da qualidade de sua empresa. Alguns ainda perdem o sono com as fiscalizações das Vigilâncias Sanitárias e seu enorme volume de documentos e registros exigidos.
O principal documento normativo do segmento de produtos para saúde (correlatos) é a RDC 665/2022, que é uma resolução que estabelece requisitos aplicáveis à fabricação e armazenamento de produtos médicos e produtos para diagnóstico de uso in vitro, para assegurar que os mesmos sejam seguros e eficazes.
De uma forma bastante abrangente, estes requisitos constituem a certificação em Boas Práticas de Fabricação – BPF, para as empresas fabricantes de produtos médicos, descrevendo os métodos de controle de qualidade nos processos de compra, fabricação, embalagem, rotulagem, armazenamento, distribuição, instalação e assistência técnica. Para as empresas importadoras e distribuidoras desses produtos, a certificação é constituída pelas Boas Práticas de Armazenamento e Distribuição – BPAD.
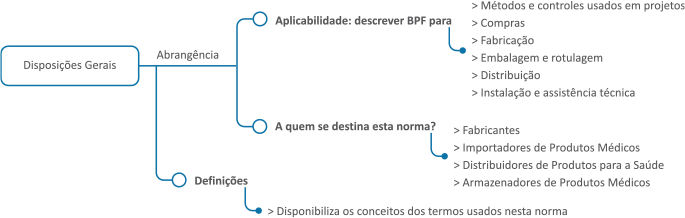
Para auxiliar no controle da qualidade, esta RDC determina que essas empresas devem estabelecer e manter um sistema de qualidade com procedimentos eficazes e que contenham instruções claras sobre todas as atividades relacionadas a ele, bem como estabelece também a criação de procedimentos que atestem o cumprimento dos dispositivos legais previstos na legislação sanitária brasileira e que esses dispositivos estejam de acordo com o previsto nesta norma.
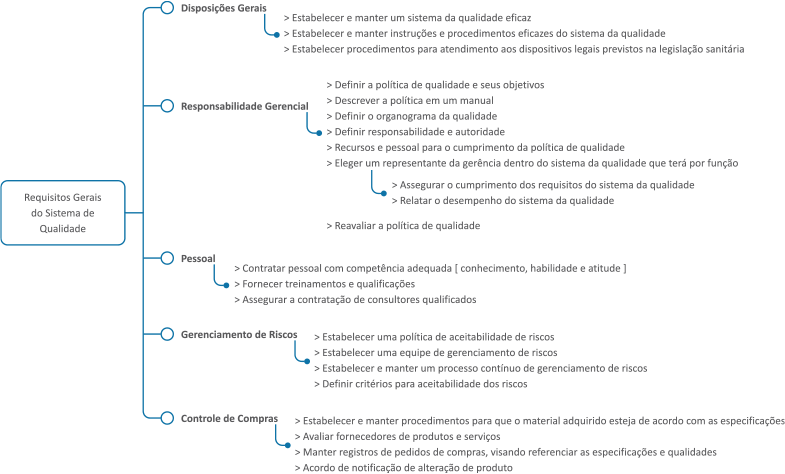
Um Sistema de Gestão da Qualidade, segundo a ISO - International Organization for Standardization, é determinado como um conjunto de elementos inter-relacionados ou interativos para o estabelecimento de políticas e objetivos, com atenção voltada à gestão da qualidade dos processos.
É de responsabilidade gerencial não só a definição da política de qualidade, mas também a criação de um manual que deverá auxiliar na implantação dessa política dentro da empresa. Deverá ser criada uma estrutura que seja responsável pela gestão da qualidade. Esta estrutura deverá estar dentro do organograma da empresa e ter pessoal em número e qualificação suficiente para gerir o sistema da qualidade.
As responsabilidades e atribuições devem ser outorgadas pela gerência, que também se comprometerá com a estrutura da qualidade, elegendo um representante dentro dessa estrutura. Cabe ao representante da gerência fazer cumprir os requisitos do sistema da qualidade e relatar o desempenho do mesmo. Baseado nessas informações, cabe à gerência fazer as reavaliações da política de qualidade, visando a sua melhoria contínua.
Todo pessoal interno, ou externo, empregados ou prestadores de serviço que estejam inseridos diretamente em atividades relacionadas ao sistema da qualidade, devem ter experiência comprovada. O sistema da qualidade, por sua vez, deve prever o treinamento e qualificação de funcionários, além de elaborar e manter documentos que registrem estes treinamentos.

A RDC nº 665/2022 determina que cada fabricante deve elaborar e manter um sistema de gerenciamento de riscos, assim como definir critérios para aceitação dos mesmos. O risco é um evento ou uma condição incerta que, caso ocorra, tem um efeito em alguma parte do processo. Os riscos têm origem nas incertezas existentes em todos os processos e no uso do produto. Os conhecidos são aqueles que foram identificados e analisados, possibilitando o planejamento das respostas. Os riscos que não podem ser gerenciados de forma proativa devem conter um plano de contingência. O gerenciamento de riscos deve ser elaborado com base na ISO 14971.

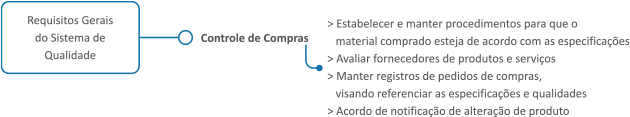
A empresa deve assegurar que comprará apenas de fornecedores e prestadores de serviços qualificados de acordo com critérios documentais e de qualidade. A RDC nº 665/2022 coloca como requisito do sistema de qualidade o controle de compras, estabelecendo que o fabricante deve criar e manter um procedimento para que o material adquirido esteja de acordo com as especificações e manter um registro de compra com o objetivo de referenciar as especificações de qualidade. O fabricante deve ter um acordo com fornecedor de material para que qualquer alteração seja imediatamente comunicada ao fabricante, para que este avalie o impacto dessas mudanças no produto.

Insira seu nome e e-mail para baixar esse conteúdo gratuitamente